Перейти к:
Термодинамическое моделирование восстановления кобальта и никеля при использовании концентратов гидрометаллургического обогащения для легирования стали
https://doi.org/10.17073/0368-0797-2024-4-384-390
Аннотация
В статье приведены исследования восстановительных процессов в модельных термодинамических системах и процессов восстановления никеля из никелевого концентрата и кобальта и никеля из кобальт-никелевого концентрата. Концентраты получены при гидрометаллургическом обогащении полиметаллических марганецсодержащих руд Кемеровской обл. – Кузбасса. Методом термодинамического моделирования с использованием программного комплекса Терра определено, что никель из оксида можно полностью восстановить в системе NiO – C при расходе углерода 0,08 кг/кг NiO и при расходе углерода 0,15 кг/кг NiO в системе NiO – Fe2О3 – C. Восстановление кобальта в системе СоО – С начинается при температуре около 513 К при любых расходах углерода. С дальнейшим ростом температуры процесс восстановления зависит только от расхода восстановителя. Из полученных данных термодинамического моделирования следует, что восстановление кобальта из кобальт-никелевого концентрата начинается при температуре примерно 513 К и в дальнейшем от температуры зависит незначительно. Степень извлечения кобальта возрастает с увеличением количества восстановителя при температурах до 553 К, затем остается постоянной до температуры 1473 К. Восстановление никеля протекает при температуре выше 473 К. Степень восстановления никеля слабо зависит от температуры и количества восстановителя при его расходе более 0,02 кг/кг концентрата. Проведенные лабораторные исследования показали, что в период плавления можно восстановить никель из его оксида твердым углеродом практически полностью, так как никель обладает меньшим сродством к кислороду, чем железо. Теоретические и экспериментальные исследования прямого легирования стали показали, что при восстановлении никеля и кобальта целесообразно использовать твердофазный процесс. Концентрат никеля и кобальт-никелевый концентрат при выплавке стали в электропечи желательно вводить в завалку в виде смесей, окомкованных с углеродистым восстановителем.
Ключевые слова
Для цитирования:
Рыбенко И.А., Нохрина О.И., Рожихина И.Д., Голодова М.А. Термодинамическое моделирование восстановления кобальта и никеля при использовании концентратов гидрометаллургического обогащения для легирования стали. Известия высших учебных заведений. Черная Металлургия. 2024;67(4):384-390. https://doi.org/10.17073/0368-0797-2024-4-384-390
For citation:
Rybenko I.A., Nokhrina O.I., Rozhikhina I.D., Golodova M.A. Thermodynamic modeling of cobalt and nickel reduction using hydrometallurgical enrichment concentrates for steel alloying. Izvestiya. Ferrous Metallurgy. 2024;67(4):384-390. https://doi.org/10.17073/0368-0797-2024-4-384-390
Актуальность
Современные технологии должны соответствовать определенным требованиям, основными из которых являются:
– рациональное использование материальных и энергетических ресурсов;
– расширение номенклатуры продукции;
– повышение качества продукции;
– экологическая безопасность.
Все эти проблемы в значительной мере присущи производству черных металлов. Большое значение имеют получение более дешевыми методами и в больших количествах особо чистой стали с низким содержанием нежелательных примесей; изменение структуры и типа потребляемых легирующих и раскислителей в сторону снижения требований к составу и соответствующее их удешевление.
Анализ современной технологии выплавки стали показывает, что наиболее весомыми статьями в себестоимости металла являются затраты на раскисление и легирование стали, а также технологическую энергию. Одним из путей решения задачи повышения эффективности производства стали является изменение технологии получения легирующих с переходом к прямому легированию стали в печи или в ковше с использованием руд и концентратов [1; 2].
В последние два десятилетия как в России [3 ‒ 5], так и за рубежом [6 – 8] уделяется большое внимание поискам новых химических и гидрометаллургических методов обогащения бедных руд (в том числе марганцевых) в связи с решением проблемы ресурсосбережения. При комплексном обогащении полиметаллических марганецсодержащих руд Кузбасса по технологии, предложенной в работе [9], наряду с высококачественным марганцевым и железосодержащим концентратами получаются концентраты цветных металлов (никелевый концентрат, а также никель-кобальтовый), которые могут быть использованы для прямого легирования.
Технический прогресс в машиностроении, строительстве, химии и других отраслях промышленности обуславливает повышение спроса на качественные стали и сплавы. Наиболее востребованными являются конструкционные, жаропрочные, кислотоустойчивые и нержавеющие марки сталей, при производстве которых используются цветные металлы (одним из основных является никель).
Запасы богатых никелевых руд с содержанием никеля около 4 % ограничены, поэтому в производство вовлекают бедные силикатные руды с содержанием никеля до 1,5 % [10 ‒ 12]. В настоящее время уделяется большое внимание поискам новых способов обогащения и использования никельсодержащих руд [13 ‒ 15]. В связи с этим в качестве альтернативного сырья можно рассматривать полиметаллические марганецсодержащие руды и железомарганцевые конкреции, в которых содержание никеля достигает 0,5 % [16; 17].
Ежегодное мировое производство никеля сохраняется на уровне 1 млн т. В условиях глобальной мировой экономики спрос на никель продолжает расти, несмотря на постоянное повышение его цены. Постоянно растущий спрос на никель обусловлен широкими возможностями его использования. Большая часть произведенного никеля используется для легирования стали.
Возрастающая потребность различных областей науки и техники в кобальте, обусловленная развитием аэрокосмической отрасли, производства спецсталей для оборудования нефтедобывающей промышленности, вызывают необходимость увеличения объема его производства. Основная доля получаемого кобальта расходуется на изготовление различных сплавов. Кобальт чаще всего применяется в сплавах с железом, хромом, вольфрамом и молибденом. Он повышает режущие свойства быстрорежущей стали, поэтому нашел применение в инструментальной промышленности.
Кобальтовые сплавы обладают хорошими магнитными свойствами, коррозионной стойкостью, износостойкостью и высокой термостойкостью.
Добавление кобальта в сталь позволяет сохранять магнитные свойства при высоких температурах и вибрациях, а также увеличивает сопротивление размагничиванию. Так, например, японская сталь, содержащая до 60 % Cо, имеет большую коэрцитивную силу и всего лишь на 2,0 ‒ 3,5 % теряет магнитные свойства при вибрациях. Магнитные сплавы на основе кобальта применяют при производстве сердечников электромоторов, трансформаторов и в других электротехнических устройствах [18; 19].
Анализ достоинств и недостатков прямого легирования стали показывает, что перспективность той или иной технологии определяется такими технико-экономическими показателями, как длительность плавки и расход восстановителя. В процессе исследований ставилась задача максимальной замены кремния – основного восстановителя легирующих элементов из концентратов, более дешевым восстановителем углеродом, и получение стабильного извлечения никеля и кобальта из оксидов, входящих в состав концентратов, полученных при гидрометаллургическом обогащении полиметаллических марганецсодержащих руд.
Методика исследований и материалы
В условиях выплавки стали в дуговых электропечах на разных этапах плавки в качестве восстановителей могут рассматриваться углерод, оксид углерода и кремний, растворенные в жидкой стали. Для определения условий восстановления легирующих элементов из концентратов использовали методы термодинамического моделирования на основе расчета равновесных состояний в модельных термодинамических системах [20]. При реализации термодинамического моделирования в настоящей работе использовали готовые программные продукты (программный комплекс Терра), разработанные в Московском государственном техническом университете, позволяющие на основе принципа максимума энтропии находить равновесный состав многокомпонентной, гетерогенной термодинамической системы для высокотемпературных условий.
Элементарная система формируется путем задания количества составляющих ее компонентов и температуры. При необходимости формируются составы конденсированных растворов. При выбранных двух термодинамических параметрах реализуются многовариантные расчеты равновесных составов в зависимости от термодинамических параметров или расходов исходных материалов.
Набор веществ, который может образовываться при заданном элементном составе смеси, определялся в результате численного моделирования для выбранного диапазона температур и различных термодинамических состояний. Из полного перечня возможных веществ были выбраны только те вещества, концентрации которых превышали 10\(^‒\)4 моль/кг смеси. Расчет проводили в интервале температур от 573 до 1873 К, соответствующим температурам выплавки стали.
Термодинамическое моделирование восстановления никеля, кобальта и совместно никеля и кобальта проводили для чистых систем и концентратов, полученных при обогащении полиметаллического марганцевого сырья: никелевый концентрат (45,0 % Ni; 2,3 % Mn; 1,4 % Fe; 0,5 % Co; 0,1 % Cu; менее 0,015 % P; следы SiO2 и 2,82 % п.п.п.); кобальт-никелевый концентрат (76,8 % CoO; 11,9 % NiO; 4,9 % Fe2O3 ; 1,2 % Mn2O3 ; 0,2 % SiO2 ; 1,2 % CaCl2 ; 3,8 % п.п.п.) и кокс ОАО «ЕВРАЗ Объединенный Западно-сибирский металлургический комбинат» (A\(^d\) = 13,6 %; V\(^{daf}\) = 2 %; W\(^p\) = 2 %; 51,1 % SiO2 ; 23,3 % Al2O3 ; 0,16 % MnO2 ; 1,58 % MgO; 1,2 % CaO; 17,46 % Fe2O3 ; 0,5 % P2O5 ; 1,2 % K2O; 0,2 % Na2O; 74,4 % СО2 ).
В ходе лабораторных исследований был экспериментально определен и опробован способ ввода оксида никеля в дуговую электропечь. Сталь выплавляли в дуговой лабораторной печи вместимостью 10 кг. Из никелевого концентрата, полученного при обогащении полиметаллических марганцевых руд фракцией менее 0,5 мм и коксовой мелочи, были изготовлены окатыши диаметром 20 – 30 мм. Окатыши загружали в печь по двум вариантам: I – в завалку; II – в восстановительный период на «зеркало» металла перед наведением шлака.
Расчет количества окатышей вели на содержание никеля в стали 1 %. Экспериментальные плавки вели по классической двухшлаковой технологии. При выплавке стали использовали металлический лом состава, мас. %: 0,275 C; 0,267 Si; 0,423 Mn; 0,175 Cr; 0,1 Ni; 0,027 S; 0,028 Р; остальное Fe. Масса шихтовых материалов для опытных плавок приведена в таблице. По окончании плавки отбирали пробы металла и шлака на химический анализ. Выпуск металла и шлака осуществляли в ковш. Полученный слиток разрезали по высоте на три равные части и анализировали металл.
Исходные шихтовые материалы для опытных плавок
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
Обсуждение результатов
Восстановление никеля из оксидов никелевого концентрата
Расчет возможных составов, получающихся в результате протекания процессов восстановления никеля в термодинамической системе, состоящей из элементов NiO – C, осуществляли изменением содержания углерода в системе, что позволило оценить границы концентрационных областей восстановительных процессов. Модельную систему NiO – C формировали путем задания исходного состава смеси 1 кг оксида NiO и углерода в количестве от 0,01 до 0,1 кг/кг оксида. Исследования проводили в интервале температур от 1073 до 1873 К. Зависимости коэффициентов извлечения никеля из оксида от количества углерода при температурах 1073, 1473 и 1873 К представлены на рис. 1. Термодинамические расчеты показали, что максимальное восстановление никеля достигается при расходе углерода 0,08 кг/кг NiO. Следовательно, полного восстановления никеля можно достичь при твердофазном восстановлении до появления жидкой фазы.
Рис. 1. Зависимости параметров восстановления никеля от количества углерода |
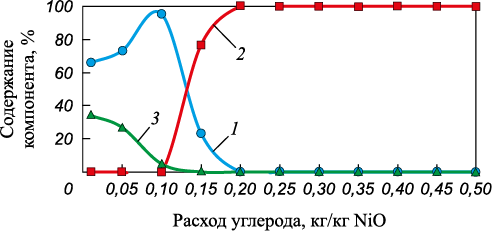
Результаты расчетов равновесных состояний системы NiO – Fe2О3 – C в пределах изменения углерода 0,01 – 0,5 кг/кг NiO и исходном количестве оксидов NiO (1 кг), Fe2O3 (2 кг) представлены на рис. 2. В качестве значимых оказалась конденсированная фаза, состоящая из Ni, NiO, С, FeO и Fe2О3 . Газовая фаза представлена оксидами СО и СО2 .
Рис. 2. Зависимость состава шлаковой фазы от расхода углерода |
Шлаковая фаза рассматриваемой системы представлена оксидами FeO, Fe2О3 и NiO. При введении восстановителя в количестве более 0,2 кг/кг NiO шлаковая фаза системы состоит только из оксида железа FeO. Полное восстановление никеля из оксида происходит при содержании углерода 0,15 кг/кг NiO в системе NiO – Fe2О3 – C.
Результаты термодинамического моделирования показали, что никель из оксида можно полностью восстановить как в системе NiO – C, так и в системе NiO – Fe2О3 – C при температурах металлургических процессов.
В ходе лабораторных исследований был экспериментально определен оптимальный способ ввода оксида никеля в дуговую электропечь. В плавках 1 – 3 использовали окатыши, изготовленные из никелевого концентрата, в 4 – 6 – смеси никелевого концентрата и кокса (см. таблицу).
Результаты опытных плавок легирования стали с использованием никельсодержащих окатышей показали, что извлечение никеля из концентрата составило 92 – 95 % (вариант I), 75 – 78 % (вариант II).
Снижение извлечения никеля при присадке его в начале восстановительного периода, по-видимому, связано с его частичным испарением: при попадании в зону дуг никель восстанавливается и может частично испаряться, так как имеет относительно низкую температуру кипения.
В условиях выплавки стали в дуговой электропечи в интервале температур 1173 – 1873 К в период плавления практически полностью можно восстановить никель из его оксида твердым углеродом, так как никель обладает меньшим сродством к кислороду, чем железо.
Восстановление кобальта в элементарных системах
Исследование процесса диссоциации оксидов кобальта показало, что высший оксид кобальта Со2О3 отсутствует в системе при температурах выше 473 К. Устойчивый при комнатной температуре оксид кобальта представляет собой сложный оксид Co3O4 , имеющий структуру шпинели. В его кристаллической структуре одна часть узлов занята ионами Co\(^{2+}\), а другая ‒ ионами Co\(^{3+}\); он разлагается с образованием CoO при температуре выше 1173 К. Результаты термодинамических расчетов приведены на рис. 3. Из представленных зависимостей следует, что оксид Со3О4 остается устойчивым до температуры 1173 К. В интервале температур от 1173 до 1223 К количество оксида Со3О4 снижается до нуля, при температуре 1173 К появляется оксид СоО и при температуре 1223 К его количество становится максимальным, устойчивым к изменению температуры.
Рис. 3. Термическая диссоциация оксидов кобальта: |
При моделировании восстановления кобальта рассматривали систему СоО ‒ С. Расчеты проведены в интервале температур от 273 до 1273 К и при расходе восстановителя (углерода) от 0,02 до 0,1 кг/кг СоO. Термодинамическое моделирование показало, что восстановление кобальта начинается при температуре около 513 К при любых расходах углерода. С дальнейшим ростом температуры процесс восстановления зависит только от расхода восстановителя (рис. 4). Кобальт полностью восстанавливается из оксида при расходе углерода 0,1 кг/кг СоО при температуре 1273 К.
Рис. 4. Зависимость количества восстановленного кобальта |
Термодинамические расчеты восстановления кобальта в системах Со ‒ О ‒ Si и Co ‒ O ‒ Al в интервале температур от 273 до 1273 К показали, что он полностью восстанавливается при расходе кремния 0,1 кг/кг СоO или при расходе алюминия 0,24 кг/кг СоО при температуре 1273 К.
Восстановление никеля и кобальта из кобальт-никелевого концентрата
Было также исследовано восстановление кобальта и никеля из оксидов концентрата коксом в интервале температур от 273 до 2073 К. Расход кокса варьировался от 0,02 до 0,1 кг/кг концентрата.
В составе продуктов восстановления в значимых количествах присутствовали:
– кобальт, никель, оксиды кобальта, никеля, железа, марганца, силикаты и алюминаты кальция и магния (конденсированная фаза);
– пары воды, оксиды СО и СО2 , хлориды металлов (газовая фаза); хлориды определяли при температурах выше 1513 К.
Зависимости коэффициентов извлечения кобальта и никеля из кобальт-никелевого концентрата от температуры и расхода углерода приведены на рис. 5.
Рис. 5. Зависимости коэффициентов извлечения никеля (а) |
Из полученных термодинамических данных следует, что восстановление кобальта начинается при температуре примерно 513 К и в дальнейшем от температуры зависит незначительно. Степень извлечения кобальта возрастает с увеличением количества восстановителя при температурах до 553 К, затем остается постоянной до температуры 1473 К. С дальнейшим ростом температуры извлечение кобальта снижается. При расчете коэффициента извлечения кобальта учитывался только кобальт, содержащийся в конденсированной фазе. В газовой фазе присутствует соединение CoCl2 , количество которого возрастает с увеличением температуры.
Восстановление никеля протекает при температуре выше 473 К. Степень восстановления никеля слабо зависит от температуры и количества восстановителя при расходе последнего выше 0,02 кг/кг концентрата.
Результаты исследования показали, что при восстановлении никеля и кобальта из концентратов полное восстановление этих элементов достигается при температурах твердофазного восстановления в интервале 573 ‒ 1073 К. Полученные данные согласуются с результатами работ [18; 19].
Выводы
Из результатов теоретических и экспериментальных исследований следует, что при восстановлении никеля и кобальта целесообразно использовать твердофазный процесс. Никель углеродом из никелевого концентрата можно полностью восстановить при температуре 1073 К, восстановление кобальта и никеля из кобальт-никелевого концентрата начинается при температуре примерно 513 К и в дальнейшем от температуры зависит незначительно. Следовательно, концентрат никеля и кобальт-никелевый концентрат при выплавке стали в электропечи целесообразно вводить в завалку в виде окомкованных с углеродистым восстановителем смесей.
Список литературы
1. Нохрина О.И., Рожихина И.Д., Дмитриенко В.И. Платонов М.А. Легирование и модифицирование стали с использованием природных и техногенных материалов. Томск: Изд-во Томского политехнического университета; 2013:320.
2. Носов Ю.Н., Камшуков В.П., Соколов В.В. и др. Прямое легирование стали марганцевым агломератом в ковше на выпуске из конвертера. Сталь. 2004;(5):35–36.
3. Нохрина О.И., Рожихина И.Д., Едильбаев А.И., Едильбаев Б.А. Марганцевые руды Кемеровской области ‒ Кузбасса и методы их обогащения. Известия вузов. Черная металлургия. 2020;63(5):344–350. https://doi.org/10.17073/0368-0797-2020-5-344-350
4. Чернобровин В.П., Мизин В.Г., Сирина Т.П., Дашевский В.Я. Комплексная переработка карбонатного марганцевого сырья: химия и технология. Челябинск: ЮУрГУ; 2009:294.
5. Курков А.В., Мамошин М.Ю., Рогожин А.А. Прорывные гидрометаллургические процессы для устойчивого развития технологий переработки минерального сырья. Москва: Научное издание ФГБУ «ВИМС»; 2019:106.
6. Pan M.C., Liu X.L., Zou R., Huang J., Han J.C. Study of heat treatment technology on medium-carbon-low-alloy-steel large hammer formation of gradient performance. Advanced Materials Research. 2014;881-883:1288–1292. http://dx.doi.org/10.4028/www.scientific.net/AMR.881-883.1288
7. Sun D., Li M.L., Li C.H., Cul R., Zheng X.Y. A green enriching process of Mn from low grade ore of manganese carbonate. Applied Mechanics and Materials. 2014;644–650: 5427–5430. http://dx.doi.org/10.4028/www.scientific.net/AMM.644-650.5427
8. Ayala J., Fernandez B. Recovery of manganese from silicomanganese slag by means of a hydrometallurgical process. Hydrometallurgy. 2015;158:68–73. https://doi.org/10.1016/j.hydromet.2015.10.007
9. Нохрина О.И., Рожихина И.Д., Рыбенко И.А., Голодова М.А., Израильский А.О. Гидрометаллургическое обогащение полиметаллических и железомарганцевых руд. Известия вузов. Черная металлургия. 2021;64(4): 273–281. https://doi.org/10.17073/0368-0797-2021-4-273-281
10. Pat. 7125436 USA, IPC7 from 22 at 15/00, from 22 at 11/08. The method of autoclave leaching of nickel ores. Run L., Maurt T. No. 10/907324. Published on 10.24.2006. NPC 75/724.
11. Wang K., Li J, McDonald R.G., Browner R.E. The effect of iron precipitation upon nickel losses from synthetic atmospheric nickel laterite leach solutions: Statistical analysis and modeling. Hydrometallurgy. 2011;109(1-2):140–152. http://dx.doi.org/10.1016/j.hydromet.2011.06.009
12. Anjum F., Shahid M., Akcil A. Biohydrometallurgy techniques of low grade ores: A review on black shale. Hydrometallurgy. 2012;117–118:1–12. http://dx.doi.org/10.1016/j.hydromet.2012.01.007
13. Giannopoulou I., Panias D. Differential precipitation of copper and nickel from acidic polymetallic aqueous solutions. Hydrometallurgy. 2008;90(2–4):137–146. https://doi.org/10.1016/j.hydromet.2007.10.004
14. 1731623 EVP, IPC from 22 to 23/00. Method for teaching and extraction of nickel and cobalt. H. Yakushiji, S. Ito, K. Jura, M. Shimamori. Published on 12.13.2006.
15. Coto O., Galizia F., Hernandez I., Marrero J., Donati E. Cobalt and nickel recoveries from laterite tailings by organic and inorganic bioacids. Hydrometallurgy. 2008; 94(1–4):18–22. http://dx.doi.org/10.4028/www.scientific.net/AMR.20-21.107
16. Ntuli F., Lewis A.E. Kinetic modelling of nickel powder precipitation by high-pressure hydrogen reduction. Chemical Engineering Science. 2009;64(9):2202–2215. http://dx.doi.org/10.1016/j.ces.2009.01.026
17. Прошунин И.Е., Нохрина О.И. Комплексное извлечение ценных компонентов из железомарганцевых конкреций. Известия вузов. Черная металлургия. 2009;52(8):17–19.
18. Козлов П.А. Исследование влияния легирования на состав жаропрочных 9 %-ных хромистых сталей для элементов теплоэнергетического оборудования: автореф. дис… канд. техн. наук: 05.16.02. Москва; 2011:25.
19. Книсс В.А. Физико-химические основы и технология восстановительной плавки закиси-окиси кобальта в электропечах постоянного тока: автореф. дис… канд. техн. наук: 05.16.02. Екатеринбург; 2008:31.
20. Трусов Б.Г. Программная система ТЕРРА для моделирования фазовых и химических равновесий при высоких температурах. В кн.: III межд. симпозиум «Горение и плазмохимия». 24–26 августа 2005. Алматы, Казахстан. Алматы: Казак университетi; 2005:52–57.
Об авторах
И. А. РыбенкоРоссия
Инна Анатольевна Рыбенко, д.т.н., профессор, заведующий кафедрой прикладных информационных технологий и программирования
Россия, 654007, Кемеровская обл. – Кузбасс, Новокузнецк, ул. Кирова, 42
О. И. Нохрина
Россия
Ольга Ивановна Нохрина, д.т.н., профессор кафедры металлургии черных металлов и химической технологии
Россия, 654007, Кемеровская обл. – Кузбасс, Новокузнецк, ул. Кирова, 42
И. Д. Рожихина
Россия
Ирина Дмитриевна Рожихина, д.т.н., профессор-консультант кафедры металлургии черных металлов и химической технологии
Россия, 654007, Кемеровская обл. – Кузбасс, Новокузнецк, ул. Кирова, 42
М. А. Голодова
Россия
Марина Анатольевна Голодова, к.т.н., доцент кафедры архитектуры
Россия, 654007, Кемеровская обл. – Кузбасс, Новокузнецк, ул. Кирова, 42
Рецензия
Для цитирования:
Рыбенко И.А., Нохрина О.И., Рожихина И.Д., Голодова М.А. Термодинамическое моделирование восстановления кобальта и никеля при использовании концентратов гидрометаллургического обогащения для легирования стали. Известия высших учебных заведений. Черная Металлургия. 2024;67(4):384-390. https://doi.org/10.17073/0368-0797-2024-4-384-390
For citation:
Rybenko I.A., Nokhrina O.I., Rozhikhina I.D., Golodova M.A. Thermodynamic modeling of cobalt and nickel reduction using hydrometallurgical enrichment concentrates for steel alloying. Izvestiya. Ferrous Metallurgy. 2024;67(4):384-390. https://doi.org/10.17073/0368-0797-2024-4-384-390