Перейти к:
Термодинамическое моделирование процесса восстановления железорудных материалов водородсодержащими газами
https://doi.org/10.17073/0368-0797-2025-2-163-170
Аннотация
В статье представлены результаты исследования процессов восстановления железорудных титаномагнетитовых окатышей синтез-газом с помощью термодинамического моделирования с использованием программного комплекса «Терра». Его применение позволило смоделировать и спрогнозировать химические и фазовые превращения в железорудных титаномагнетитовых окатышах при восстановлении с использованием водородсодержащего синтез-газа, учитывая влияние температуры, концентрации водорода и других параметров. Расчеты проводились с различным содержанием газовой смеси для оценки эффективности модели. Содержание газовой смеси CO – N2 – H2 – СН4 для расчетов изменялось с увеличением CO и H2 , уменьшением N2 и постоянным СН4 . Термодинамическое моделирование показало, что при достижении баланса основных фаз в высокотемпературных системах при восстановлении различными газовыми смесями концентрация распределения кремния, алюминия, титана, магния и кальция остается постоянной. Значительные изменения наблюдаются в концентрации содержания железа, ванадия и марганца, что связано с особенностями процесса восстановления и составом используемых газов. Получены зависимости равновесного состава системы от температуры при различных содержаниях элементов. Построенная термодинамическая модель описывает процесс восстановления и может быть использована для оптимизации данного процесса в различных условиях производства.
Ключевые слова
Для цитирования:
Дмитриев А.Н., Бурова Ю.Е., Витькина Г.Ю., Барбин Н.М., Терентьев Д.И. Термодинамическое моделирование процесса восстановления железорудных материалов водородсодержащими газами. Известия высших учебных заведений. Черная Металлургия. 2025;68(2):163-170. https://doi.org/10.17073/0368-0797-2025-2-163-170
For citation:
Dmitriev A.N., Burova Yu.E., Vit’kina G.Yu., Barbin N.M., Terent’yev D.I. Thermodynamic modelling of reduction of iron ore materials by hydrogen-containing gases. Izvestiya. Ferrous Metallurgy. 2025;68(2):163-170. https://doi.org/10.17073/0368-0797-2025-2-163-170
Введение
В настоящее время большое внимание уделяется развитию различных способов декарбонизации металлургического производства. Классический процесс получения металла в доменных печах подразумевает выбросы в атмосферу большого объема углекислого газа. Одним из решений является движение в сторону декарбонизации без кардинальных изменений в производственном процессе, используя улавливание выбросов СО2 и их последующую утилизацию или хранение. Вторым кардинальным решением является замена СО на чистый водород или, что более выполнимо, использование синтез-газа – комбинации водорода и монооксида углерода, которая заменяет в доменном процессе значительную часть твердого углеродного топлива и создает потенциал для движения к декарбонизации, обеспечивая соблюдение высоких экологических стандартов [1 – 3].
Одним из решений задачи снижения выбросов CO2 при производстве чугуна является вдувание коксового и доменного газов в доменные печи для снижения удельного расхода кокса. Для эффективного вдувания доменного газа необходимо максимально возможное снижение содержания CO2 и H2O [4 – 5]. Коксовый газ в этом отношении гораздо более технологичен – содержание CO2 в нем составляет около 3 об. %. Например, компания ArcelorMittal анонсировала технологию вдувания коксового газа на комбинате в Испании1. Компании Dillinger и Saarstahl на комбинате Rogesa вложили 14 млн евро в строительство нового завода по конверсии коксового газа для вдувания в доменные печи2. По разным оценкам вдувание 100 м3 коксового газа на 1 т чугуна позволит снизить потребление углерода кокса на 30 кг/т чугуна.
По техническим причинам использование одного лишь водорода в доменной печи невозможно, поэтому применение водорода в схеме «доменная печь – конвертер» может расцениваться лишь как переходный шаг на пути к производству по принципу прямого восстановления железа3 [6 – 8].
Многие исследования посвящены получению богатого водородом газа при газификации различных биомасс [9 – 13]: древесный уголь, смола, углеводороды, древесина, синтетический природный газ, что на малых предприятиях становится одной из мер по снижению выбросов СО2 .
Восстановление железорудных материалов водородсодержащими газами в процессе производства чугуна сопряжено с трудностями [14 – 17]. Благодаря вычислительному эксперименту есть возможность проанализировать состояние системы, физико-химических процессов и на основе модельных представлений сделать выводы о поведении изучаемых веществ.
Исчерпание запасов традиционного передельного железорудного сырья Урала на протяжении более 300 лет ставит перед черной металлургией задачу перехода на новые виды руды. В качестве альтернативы рассматривается титансодержащее сырье, содержащее, помимо железа, ванадий и титан. Его комплексная переработка, включающая получение стали, пентаоксида ванадия, пигментного диоксида титана и титановой губки, представляет собой экономически и технологически сложную задачу, требующую оптимизации процессов извлечения всех ценных компонентов. Для ее решения, как показал опыт Института металлургии УрО РАН, перспективным направлением является применение информационных систем, описывающих физико-химические и теплофизические процессы, протекающие в металлургических агрегатах. Такие системы позволяют оптимизировать технологические параметры и повысить эффективность извлечения целевых компонентов, что имеет решающее значение для рентабельности переработки титансодержащих руд.
Целью работы является исследование термодинамики процесса восстановления железорудных титаномагнетитовых окатышей в атмосфере различных смесей газов (схожими по составу с синтез-газом, доменным, кокосовым и иными технологическими газами, содержащими водород и перспективными в плане рециклинга).
Методы исследования
В данной работе применен метод термодинамического моделирования, который заключается в анализе равновесного состояния систем. Исследования проводили с помощью программного комплекса «Терра», разработанного в МГТУ им. Н.Э. Баумана [18 – 20]. Достоинствами данного комплекса являются:
– задание условий равновесия термодинамической системы с окружающей средой любой парой термодинамических параметров (P (давление), V (удельный объем), T (температура), S (энтропия), H (энтальпия) и U (внутренняя энергия));
– проведение равновесного расчета термодинамической системы произвольного элементного состава;
– включение в число ожидаемых компонентов состава любых индивидуальных веществ за счет изменения исходных данных и определение равновесного фазового состава системы без предварительного указания термодинамически допустимых состояний;
– возможность исключения из числа компонентов равновесного состава любых веществ;
– назначение концентрации веществ с расчетом по оставшейся части системы;
– учет занимаемого конденсированного веществами объема и т.д.
Материалом для исследования послужили титансодержащие железорудные окатыши. Исходный химический состав окатышей представлен в табл. 1. Моделирование восстановления окатышей рассчитывалось для атмосферы смесей газов CO – N2 – H2 – СН4 . Составы восстановительных газов приведены в табл. 2.
Таблица 1. Исходный состав системы для восстановления газами
Таблица 2. Составы восстановительных газов
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Использованная в расчете база данных составлена на основе информации ИВТАНТЕРМО и HSC и содержит наборы термодинамических свойств как исходных компонентов газовой фазы (CO, СН4 , H2 , N2 ), так и предполагаемых продуктов их взаимодействий (CO2 , H2O и множества других), а также конденсированного углерода (графита).
В качестве двух независимых параметров использовались температура (интервал 493 – 1793 К с шагом 100 К) и давление (0,1 МПа).
Результаты исследования и их обсуждение
Исходная система при восстановлении окатышей в атмосфере водородсодержащих газов состоит из газовой и конденсированных фаз. Газовая фаза содержит CO, N2 , H2 и СН4 . Конденсированная фаза состоит из металлического раствора s1 и оксидного раствора s2.
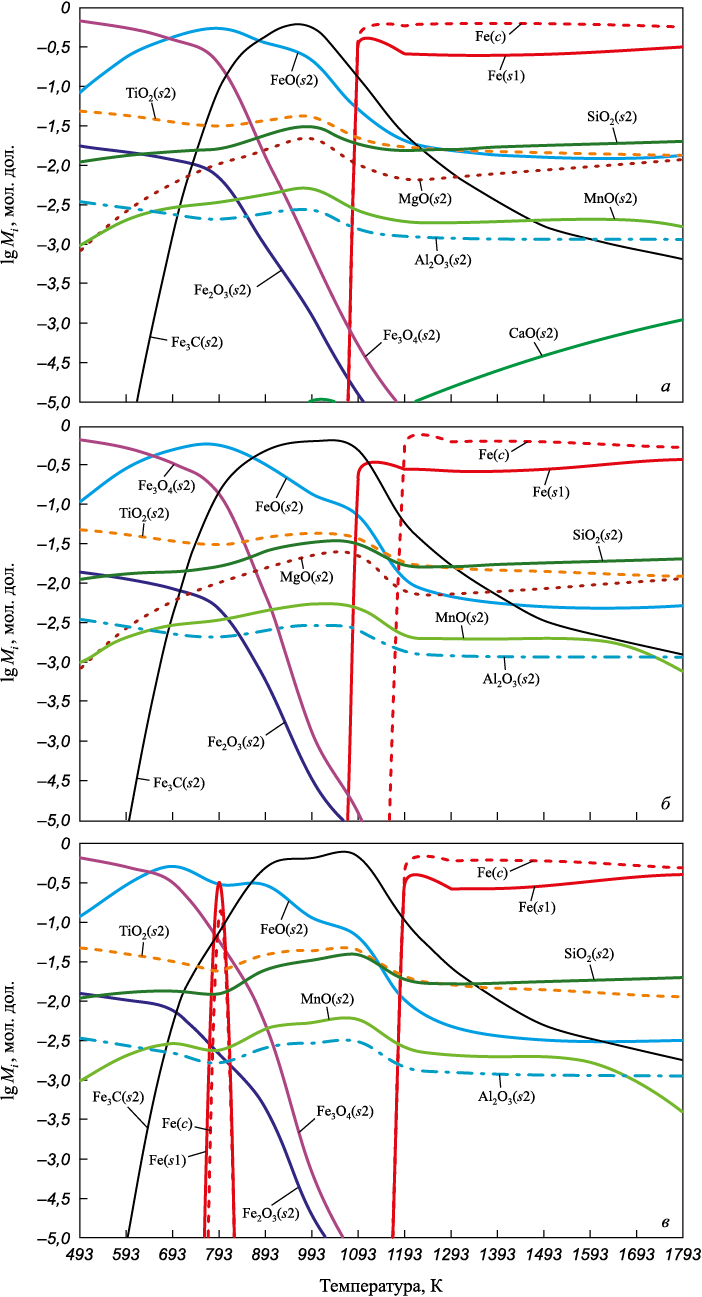
Состав оксидной конденсированной фазы представлен на рис. 1.
Рис. 1. Состав конденсированной оксидной фазы при восстановлении газом: |
Из графических данных видно, что наиболее значимыми компонентами являются Fe(s1), FeO(s2), Fe3O4(s2) с концентрацией выше 10–1 мол. дол. В интервале температур 1100 – 1793 К (рис. 1, а) преобладающим компонентом становится Fe(s1) с концентрацией 0,88 мол. дол. При восстановлении в смеси газов 2 и 3 преобладающим компонентом в интервале температур 1193 – 1793 К становится Fe(s1) (рис. 1, б, в).
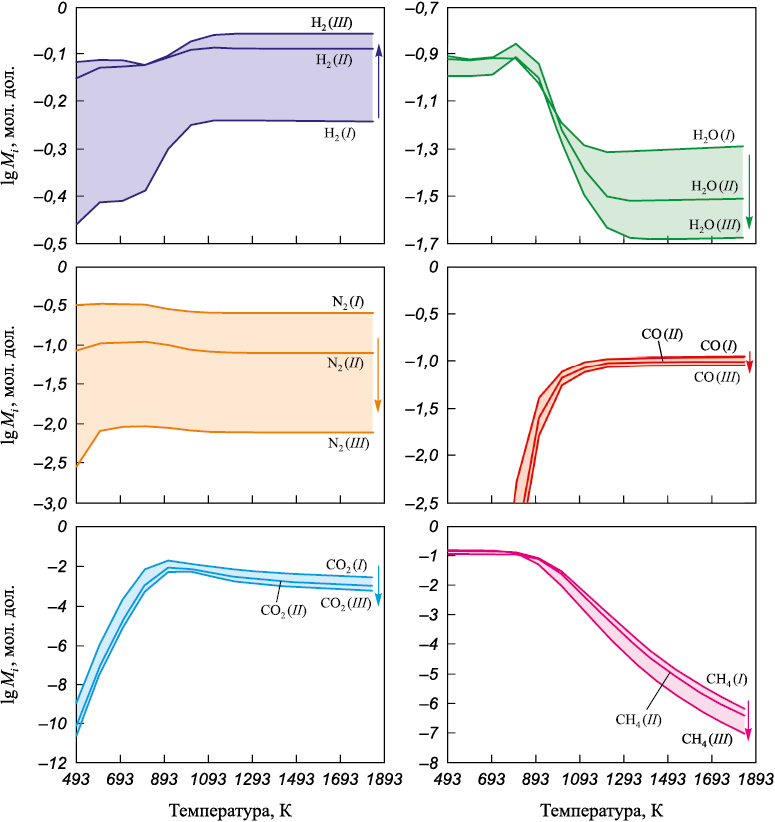
Изменения состава газовой фазы приведены на рис. 2. При температуре выше 900 К основными компонентами газовой фазы являются H2 , N2 (p ~ 0,58 атм.) и CO.
Рис. 2. Состав газовой фазы при восстановлении различными смесями газов (I, II, III) |
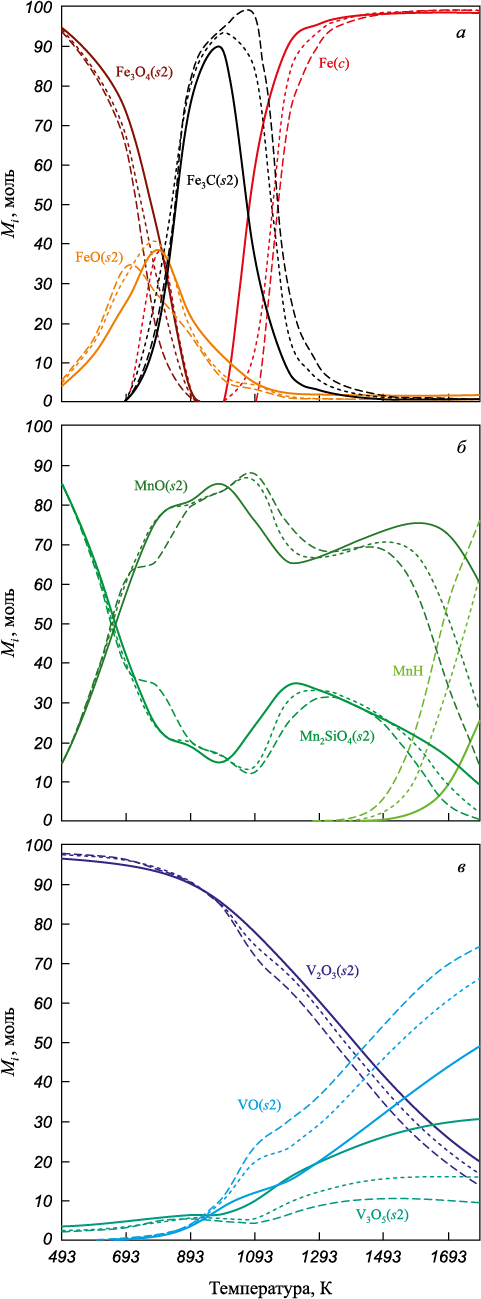
Фазовое распределение железа, ванадия и марганца в зависимости от температуры представлено на рис. 3. В температурном диапазоне 500 – 893 К преобладающей фазой железа является Fe3O4(s2), составляя от 0 до 86 мол. %. В интервале температур 593 – 993 К присутствует FeO(s2) в количестве от 11 до 40 мол. %. При температуре 993 К происходит образование карбида железа Fe3C(s2) в концентрации 88, 94 и 95 мол. %. Формирование карбида Fe3C(s2) обусловлено увеличением содержания углерода в газовой фазе, что подтверждается ростом концентрации CO и CO2 . Повышение температуры до 1000 – 1793 К приводит к появлению металлического железа Fe(s1) с концентрацией от 89 до 98 мол. %.
Рис. 3. Баланс железа (а), марганца (б), ванадия (в) |
При температуре 500 К наблюдается преобладание конденсированного силиката марганца Mn2SiO4(s2), составляющего приблизительно 85 мол. %. В диапазоне температур 593 – 1093 К происходит снижение содержания Mn2SiO4(s2) до 15, 13 и 12 мол. %, сопровождающееся увеличением концентрации конденсированного оксида марганца MnO(s2) с 34 до 86 мол. %. При дальнейшем повышении температуры до 1700 К наблюдается увеличение содержания газообразного гидрида марганца MnH до 9, 34 и 55 мол. %.
В температурном интервале 500 – 793 К преобладающей фазой ванадия является конденсированный V2O3(s2), составляющий около 96 мол. %. Повышение температуры до 1700 К приводит к плавному снижению доли V2O3(s2) до 26, 22 и 19 мол. %. Одновременно с этим наблюдается рост концентрации конденсированного оксида ванадия VO(s2) при температуре выше 893 К. Также увеличение температуры сопровождается повышением содержания конденсированного V3O5(s2) до 29, 16 и 10 мол. % при 1700 К.
В диапазоне температур от 500 до 1493 К основная часть кремния находится в виде конденсированного силиката магния MgSiO3(s2), концентрация которого составляет от 27 до 43 мол. %. Содержание силиката кальция CaSiO3(s2) (около 16 мол. %) и силиката магния Mg2SiO4(s2) (от 22 до 26 мол. %) остается практически неизменным в температурном интервале 500 – 1700 К. Повышение температуры до 1500 – 1700 К приводит к увеличению содержания конденсированного диоксида кремния SiO2(s2) до 34 мол. %.
Исследование фазового состава образца при повышении температуры от 500 до 1793 К выявило следующие закономерности. В начальном состоянии (500 К) Al2O3(s2) является преобладающей минеральной фазой алюминия, составляя 70 мол. %. При нагреве до 1700 К содержание Al2O3(s2) снижается до 58 мол. %, что свидетельствует о протекании фазовых превращений. Одновременно наблюдается увеличение концентрации MgAl2O4(s2) от 30 до 42 мол. %, что указывает на образование новой фазы. В температурном интервале 500 – 1700 К основной минеральной фазой титана является TiO2(s2). В диапазоне 993 – 1700 К содержание TiO2(s2) уменьшается с 70 до 43 мол. %. Содержание CaTiO3(s2) стабильно сохраняется на уровне 28 мол. % в пределах всего исследуемого температурного диапазона. При температуре выше 1093 К наблюдается увеличение концентрации как MgTi2O5(s2) (до 12 мол. %), так и Mg2TiO4(s2) (до 6 мол. %), что указывает на образование новых минеральных фаз. Преобладающей фазой магния в интервале 500 – 1793 К является Mg2SiO4(s2), его молярная доля составляет 43 – 54 мол. %. Нагрев до 1793 К приводит к снижению содержания Mg2SiO3(s2) с 43 до 27 мол. %. Также наблюдается незначительное повышение концентрации Mg2TiO4(s2) до 6 мол. %. При температурах от 500 до 1793 К основная часть кальция находится в виде конденсированного CaSiO3(s2) (~ 49 – 55 мол. %), CaTiO3(s2) (~45 мол. %) остается неизменным во всех трех случаях.
Таким образом, повышение температуры до 1793 К сопровождается существенной перестройкой минерального состава, что обусловлено реакциями между различными фазами. При изменении содержания CO, N2 и H2 в смеси газов концентрация распределения элементов кремния, алюминия, титана, магния и кальция остается неизменна. Значительные изменения можно наблюдать у железа, ванадия и марганца.
В интервале температур 500 – 893 К происходит уменьшение количества конденсированной фазы Fe3O4(s2), а в смеси газов 3 количество Fe3O4(s2) в интервале температур меньше, чем в смеси газов 1. Пик содержания FeO(s2) в системе при температуре 793 К в смеси газов 1 и 2 составляет ~40 мол. %, а при 693 К в смеси 1 – 34 мол. %. Пик содержания карбида Fe3C(s2) в системе при температуре 1093 К в смеси газов 3 составляет ~96 мол. %, при 993 К в смеси 2 – ~94 мол. % и в смеси 1 – ~88 мол. %. Появление Fe(s1) начинается при температуре 993 К в смеси газов 1 и 2, в смеси 3 – 1193 К. В восстановительном газе смеси 1 образование Fe(s1) больше, чем в 2 и 3.
При увеличении температуры от 1093 К содержание конденсированного V2O3(s2) и V3O5(s2) меньше, чем при смеси газов 1. Большее количество VO(s2) получается в смеси газов 3.
Количество MnO(s2) и Mn2SiO4(s2) больше при температуре от 1093 К до 1393 К в смеси газов 3, чем 1, но при температуре от 1393 К до 1793 К в смеси 1 их содержание увеличивается. Также при увеличении содержания водорода в газовой фазе возрастает количество MnH.
Выводы
Исследование термодинамических процессов косвенного восстановления титаномагнетитовых железорудных окатышей различными газовыми средами позволило установить закономерности изменения фазового состава системы в зависимости от температуры и состава восстановительной газовой смеси.
Экспериментально подтверждено, что в интервале температур 500 – 1793 К концентрации кремния, алюминия, титана, магния и кальция в равновесной системе остаются практически неизменными при использовании различных газовых смесей, содержащих CO, N2 , H2 и CH4 в разных пропорциях.
При этом наблюдается существенное изменение содержания железа, ванадия и марганца в зависимости от состава газовой смеси. Так, в смеси газов 1 (20 % CO – 65 % N2 – 10 % H2 – 5 % СН4 ) наблюдается снижение содержания карбида Fe3C(s2) и увеличение содержания Fe(s1), Fe3O4(s2), V2O3(s2), V3O5(s2), MnO(s2) и Mn2SiO4(s2) в интервале температур 1393 – 1793 К.
В смеси газов 3 (50 % CO – 5 % N2 – 40 % H2 – 5 % СН4 ) отмечается уменьшение количества Fe3O4(s2) и увеличение содержания FeO(s2), Fe3C(s2), VO(s2), MnO(s2) и Mn2SiO4(s2) в диапазоне температур 1093 – 1393 К.
Полученные результаты позволяют сделать вывод о значительном влиянии состава восстановительной газовой смеси (содержания водорода) на фазовое равновесие в системе косвенного восстановления железорудных окатышей, что имеет важное значение для оптимизации технологических процессов производства железа.
Список литературы
1. Дигонский С.В., Тен В.В. Неизвестный водород: роль водорода в полиморфизме твердых веществ, процессах твердофазного восстановления оксидов и спекания порошков. Санкт-Петербург: Наука; 2006:292.
2. Морозова О.Н., Павленко А.А., Титов С.С. Способы получения водорода. Южно-Сибирский научный вестник. 2019;(4(28)):188–194. https://doi.org/10.25699/SSSB.2019.28.46373
3. Солодова Н.Л., Минигулов Р.Р., Емельянычева Е.А. Водород как перспективный энергоноситель. Современные методы получения водорода. Вестник Казанского технологического университета. 2015;18(3):137–140. https://doi.org/10.24412/Fg4yW5JCGyE
4. Ершов Ю.Л., Шакуров А.Г., Паршин В.М., Колесников А.Г., Шишов А.Ю. Водородная эра в отечественной металлургии. Сообщение 1. Сталь. 2021;(11):50–55.
5. Ершов Ю.Л., Шакуров А.Г., Паршин В.М., Колесников А.Г., Шишов А.Ю. Водородная эра в отечественной металлургии. Сообщение 2. Сталь. 2021;(12):48–56.
6. Gao X., Zhang R., You Zh., Yu W., Dang J., Bai Ch. Use of hydrogen-rich gas in blast furnace ironmaking of V-bearing titanomagnetite: Mass and energy balance calculations. Materials. 2022;15(17):6078. https://doi.org/10.3390/ma15176078
7. Okosun T., Nielson S., Zhou Ch. Blast furnace hydrogen injection: investigating impacts and feasibility with computational fluid dynamics. JOM. 2022;74:1521–1532. https://doi.org/10.1007/s11837-022-05177-4
8. Yu X., Hu Z., Shen Y. Modeling of hydrogen shaft injection in ironmaking blast furnaces. Fuel. 2021;302:121092. https://doi.org/10.1016/j.fuel.2021.121092
9. Suopajärvi H., Pongrácz E., Fabritius T. Bioreducer use in Finnish blast furnace ironmaking – Analysis of CO2 emission reduction potential and mitigation cost. Applied Energy. 2014;124:82–93. https://doi.org/10.1016/j.apenergy.2014.03.008
10. Liu Y., Shen Ya. Modelling and optimization of biomass injection in ironmaking blast furnaces. Progress in Energy and Combustion Science. 2021;87:100952. https://doi.org/10.1016/j.pecs.2021.100952
11. Luo S., Zhou Ya., Yi Ch. Hydrogen-rich gas production from biomass catalytic gasification using hot blast furnace slag as heat carrier and catalyst in moving-bed reactor. International Journal of Hydrogen Energy. 2012;37(20):15081–15085. https://doi.org/10.1016/j.ijhydene.2012.07.105
12. Xie H., Li R., Wang Zh., Yao X., Yu Q. Hydrogen production of bio-oil steam reforming combining heat recovery of blast furnace slag: Thermodynamic analysis. International Journal of Hydrogen Energy. 2019;44(47):25514–25523. https://doi.org/10.1016/j.ijhydene.2019.08.014
13. Feliciano-Bruzual C. Charcoal injection in blast furnaces (Bio-PCI): CO2 reduction potential and economic prospects. Journal of Materials Research and Technology. 2014; 3(3):233–243. https://doi.org/10.1016/j.jmrt.2014.06.001
14. Афанасьев В.К., Горлова С.Н., Кузнецова Е.В., Сочнев А.В., Ефанов Г.И., Толстогузов В.Н., Кусков Б.А. О роли водорода в доменном процессе получения чугуна. Обработка металлов: технология, оборудование, инструменты. 2004;(4(25)):15–18.
15. Рогожников С.П., Рогожников И.С. Определение степени использования водорода в доменной печи. Черная металлургия. Бюллетень научно-технической и экономической информации. 2020;75(10):1129–1134. https://doi.org/10.32339/0135-5910-2019-10-1129-1134
16. Ялунин М.С., Витькина Г.Ю., Дмитриев А.Н., Золотых М.О., Алекторов Р.В. Оценка влияния газа-восстановителя с повышенной долей водорода на эффективность доменной плавки. В кн.: Теплотехника и информатика в образовании, науке и производстве (ТИМ'2022). Екатеринбург; 2022:185–190.
17. Шевелев Л.Н. Оценка экономической, энергетической и экологической эффективности производства чугуна и стали из рудоугольных брикетов в электросталеплавильном агрегате с использованием водородного топлива. Черная металлургия. Бюллетень научно-технической и экономической информации. 2021;77(8):918–924. https://doi.org/10.32339/0135-5910-2021-8-918-924
18. Ватолин Н.А., Моисеев Г.К., Трусов Б.Г. Термодинамическое моделирование в высокотемпературных неорганических системах. Москва: Металлургия; 1994:352.
19. Рыбенко И.А., Протопопов Е.В. Термодинамическое моделирование процессов восстановления железа. Известия вузов. Черная металлургия. 2021;64(11):825–831. https://doi.org/10.17073/0368-0797-2021-11-825-831
20. Гамов П.А., Мальков Н.В., Рощин В.Е. Термодинамическое моделирование процесса восстановления металлов из титаномагнетитовых концентратов Суроямского месторождения. Вестник Южно-Уральского государственного университета. Серия: Металлургия. 2018;18(2):21–28. http://dx.doi.org/10.14529/met180203
Об авторах
А. Н. ДмитриевРоссия
Андрей Николаевич Дмитриев, д.т.н., главный научный сотрудник лаборатории пирометаллургии восстановительных процессов
Россия, 620016, Екатеринбург, ул. Амундсена, 101
Ю. Е. Бурова
Россия
Юлия Евгеньевна Бурова, младший научный сотрудник лаборатории пирометаллургии восстановительных процессов
Россия, 620016, Екатеринбург, ул. Амундсена, 101
Г. Ю. Витькина
Россия
Галина Юрьевна Витькина, к.т.н., ведущий научный сотрудник, заведующий лабораторией пирометаллургии восстановительных процессов
Россия, 620016, Екатеринбург, ул. Амундсена, 101
Н. М. Барбин
Россия
Николай Михайлович Барбин, д.т.н., главный научный сотрудник лаборатории пирометаллургии восстановительных процессов, Институт металлургии Уральского отделения РАН; профессор, Уральский институт государственной противопожарной службы МЧС России
Россия, 620016, Екатеринбург, ул. Амундсена, 101
Россия, 620062, Екатеринбург, ул. Мира, 22
Д. И. Терентьев
Россия
Дмитрий Иванович Терентьев, к.х.н., ведущий научный сотрудник
Россия, 620062, Екатеринбург, ул. Мира, 22
Рецензия
Для цитирования:
Дмитриев А.Н., Бурова Ю.Е., Витькина Г.Ю., Барбин Н.М., Терентьев Д.И. Термодинамическое моделирование процесса восстановления железорудных материалов водородсодержащими газами. Известия высших учебных заведений. Черная Металлургия. 2025;68(2):163-170. https://doi.org/10.17073/0368-0797-2025-2-163-170
For citation:
Dmitriev A.N., Burova Yu.E., Vit’kina G.Yu., Barbin N.M., Terent’yev D.I. Thermodynamic modelling of reduction of iron ore materials by hydrogen-containing gases. Izvestiya. Ferrous Metallurgy. 2025;68(2):163-170. https://doi.org/10.17073/0368-0797-2025-2-163-170
JATS XML